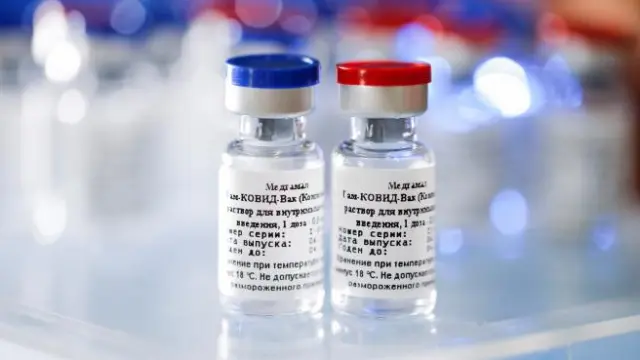
La EMA retrasa su visita a Moscú y queda en suspenso la autorización del empleo de la Spútnik V en la UE
Antes de comenzar el proceso de homologación, según la EMA, Rusia deberá presentar la correspondiente solicitud de registro de la Spútnik V, algo que, al parecer, no ha sucedido.
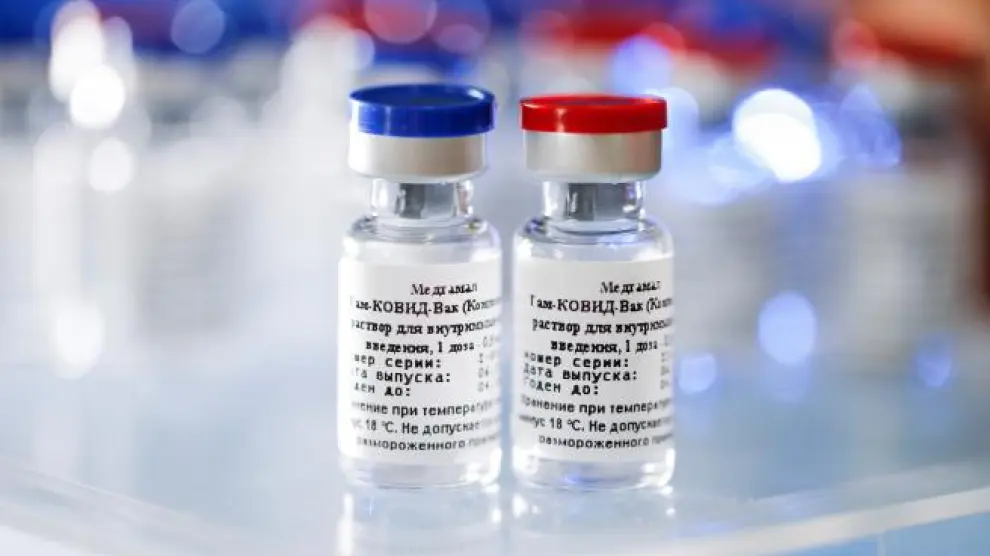
El ministro de Sanidad ruso, Mijaíl Murashko, le dijo al presidente ruso, Vladímir Putin, el pasado 22 de marzo, durante una videoconferencia dedicada a la covid-19, que especialistas de la Agencia Europea del Medicamento (EMA) llegarían a Rusia el sábado 10 de abril para evaluar la vacuna Sputnik V, elaborada por el Centro Nacional de Epidemiología y Microbiología Gamaleya de Moscú.
Tal visita se espera en la capital rusa desde hace tiempo, ya que constituye una etapa esencial de cara a autorizar el uso de la vacuna rusa en los países de la Unión Europea. Sin embargo, sigue sin producirse. A finales de marzo, el responsable del Departamento de Amenazas Sanitarias y Estrategia de Vacunación de la EMA, Marco Cavaleri, anunció que el regulador europeo enviaría una delegación a Moscú en abril. 'Financial Times' afirmó el pasado miércoles que será la presente semana cuando este grupo de especialistas europeos llegue a la capital rusa.
Según el diario ruso 'RBK', la EMA se propone efectuar en el Centro Gamaleya dos tipos de controles: el primero consistirá, según la fuente europea consultada por 'RBK', en comprobar que los productores de medicamentos que quieran ser admitidos en el mercado de la UE observen las prácticas de fabricación adecuadas, los estándares de calidad requeridos para su homologación.
El segundo tipo de inspección tiene una contenido "ético", va dirigido verificar que se han respetado los derechos, seguridad y bienestar de los participantes en los ensayos clínicos y constatar que los datos obtenidos durante estas pruebas son fiables. A este respecto, según informaciones difundidas por la agencia Reuters en diciembre, funcionarios rusos y militares involucrados en los ensayos clínicos no eran realmente voluntarios.
Kirill Dmítriev, director del Fondo Ruso de Inversiones Directas (RFPI), la organización que ha financiado la vacuna y se ocupa de su comercializarla fuera de Rusia, asegura que nadie fue presionado para que se inoculara la vacuna durante la fase de pruebas. Dmítriev dice no tener conocimiento "de ninguna preocupación por parte de la EMA (...) y sugerir que existe tal inquietud es un ejemplo claro de cómo se intenta socavar la reputación del medicamento ruso".
En cualquier caso, antes de comenzar el proceso de homologación, según la EMA, Rusia deberá presentar la correspondiente solicitud de registro de la Spútnik V, algo que, al parecer, no ha sucedido. Dmítriev afirmó que el 29 de enero fue presentada una solicitud para el registro de la vacuna, algo que la EMA desmintió días después.
El comisario europeo, Thierry Breton, encargado de gestionar la política de vacunación de la UE, cree que, incluso si la EMA aprueba el inyectable ruso y, a su juicio, "terminará haciéndolo", "llegará de todas maneras tarde al mercado europeo". Así lo estima en una entrevista a la revista alemana 'Der Spiegel'. Según sus palabras, "la homologación del medicamento no significa que se pueda producir en las cantidades necesarias inmediatamente (...) harán falta varios meses antes de que sea posible lanzar su fabricación".
"Y puesto que nuestro objetivo es vacunar a tantos europeos como sea posible de aquí al verano, la Spútnik V simplemente llegará demasiado tarde (...) la UE ya tiene suficientes vacunas registradas para lograr la inmunidad colectiva en el verano" enfatizó Breton.